Καλά νέα για την ατοπική δερματίτιδα
Τα δεδομένα παρουσιάστηκαν ως έκτακτη προφορική ανακοίνωση (late-breaking abstract) στο Ετήσιο Συνέδριο της Αμερικανικής Ακαδημίας Δερματολογίας (AAD) που πραγματοποιήθηκε στο Ορλάντο στη Φλόριδα.
“Αυτά τα νέα αποτελέσματα προστίθενται σε παλαιότερα θετικά αποτελέσματα μελετών φάσης 3 για μονοθεραπεία. Στη μελέτη CHRONOS, η χρήση του dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή έδειξε σημαντικά μεγαλύτερη υποχώρηση των δερματικών βλαβών και βελτίωση των παραμέτρων της συνολικής βαρύτητας της νόσου σε σύγκριση με μονοθεραπεία με τοπικά κορτικοστεροειδή, τα οποία χορηγούνται συνήθως για την αντιμετώπιση της μέτριας έως σοβαρής ατοπικής δερματίτιδας,” δήλωσε ο Andrew Blauvelt, M.D., Πρόεδρος του Κέντρου Ιατρικής Έρευνας του Όρεγκον και κύριος ερευνητής της μελέτης. “Αυτή η μελέτη παρουσιάζει θετικά μακροπρόθεσμα δεδομένα για το dupilumab, γεγονός ιδιαίτερα σημαντικό δεδομένου ότι η ατοπική δερματίτιδα αποτελεί μία χρόνια φλεγμονώδη νόσο. Επιπλέον, η προφορική παρουσίαση αναδεικνύει τον κρίσιμο ρόλο των κυτοκινών IL-4 και IL-13 ως βασικών παραγόντων αυτής της ατοπικής νόσου.”
Στους ασθενείς που συμπεριλήφθηκαν στη μελέτη CHRONOS η νόσος δεν ελεγχόταν με φάρμακα τοπικής εφαρμογής, συμπεριλαμβανομένων των κορτικοστεροειδών με ή χωρίς τοπικό αναστολέα καλσινευρίνης. Οι ασθενείς τυχαιοποιήθηκαν για να λάβουν dupilumab 300 mg ανά βδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή, dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή ή εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή. Η θεραπεία με dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή βελτίωσε σημαντικά παραμέτρους που σχετίζονταν με τη συνολική βαρύτητα της νόσου κατά τη 16η και την 52η εβδομάδα σέ σύγκριση με τη θεραπεία με εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
Όπως ανακοινώθηκε τον Ιούνιο του 2016, τα πρωτεύοντα καταληκτικά σημεία κατά τη 16η εβδομάδα και τα δευτερεύοντα καταληκτικά σημεία κατά την 52η εβδομάδα συνοψίζονται στα εξής:
Τη 16η εβδομάδα, το 39% των ασθενών που έλαβαν είτε dupilumab 300 mg ανά εβδομάδα με τοπικά κορτικοστεροειδή είτε dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν πλήρη υποχώρηση ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών (IGA 0 ή 1), σε σύγκριση με το 12% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 16η εβδομάδα, το 64% των ασθενών που έλαβαν dupilumab 300 mg ανά βδομάδα με τοπικά κορτικοστεροειδή και το 69% των ασθενών που έλαβαν dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση κατά 75% βάσει του δείκτη EASI, ενός δείκτη που μετρά τη βαρύτητα του εκζέματος, σε σύγκριση με το 23% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 52η εβδομάδα, το 40% των ασθενών που έλαβαν dupilumab 300 mg ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και το 36% των ασθενών που έλαβαν dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν πλήρη υποχώρηση ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών (IGA 0 or 1), σε σύγκριση με το 12,5% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 52η εβδομάδα, το 64% των ασθενών που έλαβαν dupilumab 300 mg ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και το 65% των ασθενών που έλαβαν dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση 75% βάσει του δείκτη EASI σε σύγκριση με το 22% που έλαβε εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τα νέα δεδομένα που παρουσιάστηκαν στο συνέδριο δείχνουν ότι:
Τη 16η εβδομάδα, η μέση ποσοστιαία βελτίωση βάσει του δείκτη EASI από την έναρξη της μελέτης ήταν 77% για τους ασθενείς που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και για τους ασθενείς που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, σε σύγκριση με 42% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 16η εβδομάδα, η μέση ποσοστιαία βελτίωση από την έναρξη της μελέτης της έντασης του αναφερόμενου από τον ασθενή κνησμού, βάσει της αριθμητικής κλίμακας μέτρησης του κνησμού (Pruritus Numerical Rating Scale), ήταν 55% για τους ασθενείς που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και 58% για τους ασθενείς που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, σε σύγκριση με 29% για ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 16η εβδομάδα, το 77% των ασθενών που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή ή dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχε βελτίωση ≥4 μονάδων της βαρύτητας της ατοπικής δερματίτιτδας, σύμφωνα με τη Μέτρηση Βαρύτητας Εκζέματος με βάση τον Ασθενή (POEM), ένα εργαλείο που ποσοτικοποιεί τη νόσο με βάση την εμπειρία των ασθενών, σε σύγκριση με το 37% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 16η εβδομάδα, το 74% των ασθενών που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και το 81% των ασθενών που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση ≥4 μονάδων σε παραμέτρους που σχετίζονται με την ποιότητα ζωής τους, βάσει του Δερματολογικού Δείκτη Ποιότητας Ζωής (DLQI), σε σύγκριση με το 43% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001). Ο Δερματολογικός Δείκτης Ποιότητας Ζωής (DLQI) είναι ένα ερωτηματολόγιο δέκα ερωτήσεων που χρησιμοποιείται για να αξιολογηθεί η επίπτωση της δερματικής ασθένειας στην ποιότητα ζωής του πάσχοντος.
Τη 52η εβδομάδα, το μέσο ποσοστό βελτίωσης βάσει του δείκτη EASI από την έναρξη της μελέτης ήταν 80% για ασθενείς που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και 78% για ασθενείς που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή σε σύγκριση με 46% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 52η εβδομάδα, η μέση ποσοστιαία βελτίωση από την έναρξη της μελέτης της έντασης του αναφερόμενου από τον ασθενή κνησμού, βάσει της αριθμητικής κλίμακας μέτρησης του κνησμού (NRS), ήταν 54 %για ασθενείς που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και 56 %για ασθενείς που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, σε σύγκριση με 27% για ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 52η εβδομάδα, το 64% των ασθενών που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και 76% για ασθενείς που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση ≥4 μονάδων της βαρύτητας της ατοπικής δερματίτιδας, σύμφωνα με τη Μέτρηση Βαρύτητας Εκζέματος με βάση τον Ασθενή (POEM), σε σύγκριση με το 26% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Τη 52η εβδομάδα, το 63% των ασθενών που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και το 80% των ασθενών που έλαβαν dupilumab ανά δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση ≥4 μονάδων της ποιότητας ζωής τους, βάσει Δερματολογικού Δείκτη Ποιότητας Ζωής (DLQI), σε σύγκριση με το 30% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p<0,0001).
Στη μελέτη CHRONOS, το 85% των ασθενών που έλαβαν dupilumab ανά εβδομάδα σε συνδυασμό με τοπικά κορτικοστεροειδή και το 86% των ασθενών που έλαβαν dupilumab κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή ολοκλήρωσαν έναν κύκλο θεραπείας διάρκειας 52 εβδομάδων, σε σύγκριση με το 67% των ασθενών στην ομάδα θεραπείας με εικονικό φάρμακο. Οι ασθενείς που έλαβαν dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή εμφάνισαν υψηλότερο ποσοστό αντιδράσεων στο σημείο έγχυσης (19% με dupilumab ανά εβδομάδα, 15% με dupilumab κάθε δύο εβδομάδες και 8% μόνο με τοπικά κορτικοστεροειδή) και περιπτώσεις επιπεφυκίτιδας (19% dupilumab ανά εβδομάδα, 14% dupilumab κάθε δύο εβδομάδες και 8% μόνο με τοπικά κορτικοστεροειδή).
Η αίτηση για Άδεια Βιολογικού Προϊόντος (BLA) για το dupilumab έγινε αποδεκτή προς εξέταση κατά προτεραιότητα από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) με καταληκτική ημερομηνία αξιολόγησης την 29η Μαρτίου, 2017. Ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) χαρακτήρισε το dupilumab ως Πρωτοποριακή Θεραπεία για την ανεπαρκώς ελεγχόμενη μέτρια έως σοβαρή Ατοπική Δερματίτιδα (AΔ) το 2014. Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) αποδέχτηκε προς εξέταση την Αίτηση Άδειας Κυκλοφορίας (MAA) στις 8 Δεκεμβρίου, 2016.
Το dupilumab επί του παρόντος βρίσκεται υπό κλινική ανάπτυξη και η ασφάλεια και αποτελεσματικότητά του δεν έχουν αξιολογηθεί πλήρως από καμία ρυθμιστική αρχή. Εφόσον εγκριθεί, το dupilumab θα διατεθεί στην αγορά από τη Regeneron και τη Sanofi Genzyme, την παγκόσμια επιχειρησιακή μονάδα ειδικής φροντίδας της Sanofi.
Σχετικά με την ατοπική δερματίτιδα
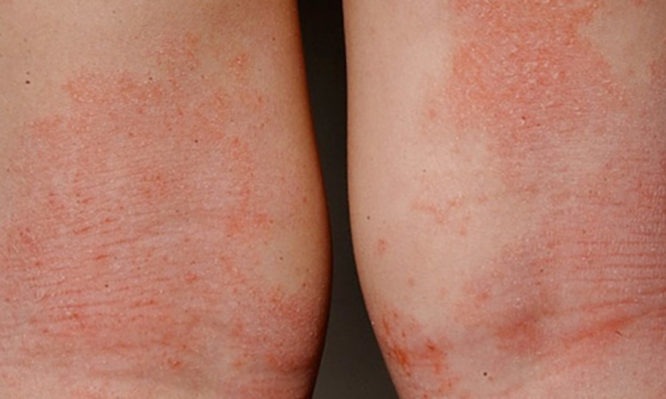
Η ατοπική δερματίτιδα (ΑΔ) είναι η πιο συνηθισμένη μορφή εκζέματος που χαρακτηρίζεται από απρόβλεπτες εξάρσεις. Πρόκειται για μία χρόνια φλεγμονώδη νόσο με συμπτώματα που είναι συχνά ορατά στην επιφάνεια του δέρματος. Η μέτρια έως σοβαρή Ατοπική Δερματίτιδα χαρακτηρίζεται από εξανθήματα και είναι δυνατό να συνοδεύεται από έντονο, συνεχή κνησμό, ξηρότητα, σκάσιμο, ερυθρότητα, δημιουργία εφελκίδων και εξιδρώματος. Ο κνησμός είναι ένα από τα πιο δύσκολα συμπτώματα των ασθενών που ενδέχεται να καταστεί εξουθενωτικό.
Υπολογίζεται ότι περίπου 300.000 άνθρωποι στις Ηνωμένες Πολιτείες υποφέρουν από ανεπαρκώς ελεγχόμενη μέτρια έως σοβαρή ατοπική δερματίτιδα και, ενώ λαμβάνουν θεραπεία, εξακολουθούν να έχουν ανάγκη για νέες θεραπευτικές επιλογές. Παρόλο που υπάρχουν διαθέσιμες θεραπείες, υφίσταται ακόμα ανεκπλήρωτη ανάγκη για θεραπείες που θα βοηθήσουν τους ενήλικες που πάσχουν από μέτρια έως σοβαρή ατοπική δερματίτιδα να διαχειριστούν τη νόσο.







